bat365正版唯一官网
邓宏魁教授荣获2024年未来科学大奖“生命科学奖”
8月16日上午,北京大学博雅讲席教授、昌平实验室领衔科学家邓宏魁被授予2024年未来科学大奖“生命科学奖”,以表彰他在开创利用化学方法将体细胞重编程为多能干细胞、改变细胞命运和状态方面的杰出工作。

未来科学大奖,是由科学家和企业家群体共同发起、着重关注原创性基础科学研究的奖项,在此之前,其“生命科学奖”曾颁发给袁隆平、施一公等著名学者,见证了我国在生命科学领域数次重大突破。今天,让我们跟随未来科学大奖的脚步,将目光转向邓宏魁。
逆转生命时钟,触摸再生之门
在生命科学领域,“再生”一直是广受关注的话题。生生不息的无限魅力,吸引着囿于时空限制的人类,以科学为工具,不断探索生命延续与修复的新篇章。科学家们寻找到的最新落点,即多能干细胞。多能干细胞具有无限增殖的特性和分化成生物体所有功能细胞类型的能力,这些神奇的特质使其在细胞治疗、药物筛选和疾病模型等领域具有广泛的应用价值,是再生医学领域最为关键的“种子细胞”。
在哺乳动物自然发育过程中,具有多能性的细胞只短暂存在于胚胎发育的早期阶段,随后便会分化为构成生物体的各种类型的成体细胞,丧失其“种子细胞”的特性。如果逆转这一自然发育过程,使高度分化的成体细胞重新获得类似胚胎发育早期的多能性状态,那么就有可能在体外制备出人的细胞、组织、器官,用于修补衰老、疾病、损伤或遗传带来的各类问题。如何逆转生命时钟,正是干细胞与再生医学领域最重要的科学问题之一。

邓宏魁(图源:中国科学杂志社)
邓宏魁团队即着眼于此,致力于开发调控细胞命运的新方法和建立制备干细胞的底层技术。2013年,团队首创了化学重编程技术,不依赖细胞内源物质,仅使用外源性化学小分子就可以逆转细胞命运,将小鼠体细胞重编程为多能干细胞,也被称为CiPS细胞,建立了化学小分子调控细胞命运的新范式。在此基础上,团队经过近十年的努力,在2022年发现了激发人成体细胞可塑性的关键方法,将“化学重编程”技术从小鼠多能干细胞制备成功地拓展应用于人多能干细胞的制备,实现了利用化学小分子将人体细胞重编程为多能干细胞,即人CiPS细胞。

邓宏魁
人CiPS技术是继“细胞核移植”和“转录因子诱导”之后新一代的、由我国自主研发的人多能干细胞制备技术。该技术的建立,突破了传统iPS技术面临的限制,具有更广阔的临床应用前景。相比传统方法,化学小分子操作简便灵活,时空调控性强、作用可逆,可以对细胞重编程过程进行精确操控。另外小分子诱导体细胞重编程技术作为非整合方法,规避了传统转基因操作引发的安全问题,有望成为更安全的临床治疗手段,为细胞治疗和器官再造提供更加简单和安全有效的方式和理想的细胞来源,也为未来再生医学的转化应用奠定了坚实基础。
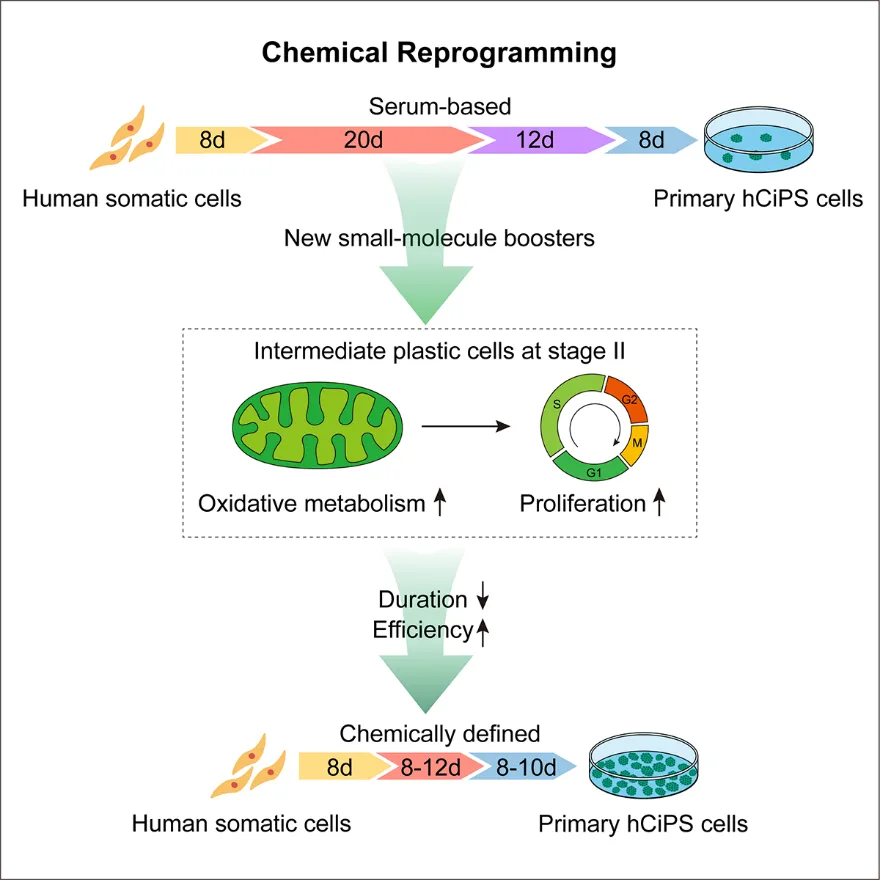
建立更加快速和高效的人体细胞化学重编程体系
从跟随到引领,促进生命科学中心转向中国
与干细胞交手十几年,在学界同仁眼中,邓宏魁是“干细胞领域的魔法师”——在北大,他带领团队不断发掘着干细胞研究的崭新学术增长点,大大拓宽了再生医学领域的研究边界,助力中国在生命科学领域处于世界领先地位。
而回到故事的最初,在邓宏魁的博士和博士后工作期间,他所研究的却并非再生医学,而是病毒学与免疫学。

邓宏魁
1997年,在邓宏魁完成博士后工作的同年,世界瞩目的多利羊出生了。这是人类使用体细胞核移植技术首次克隆了哺乳动物,它成功证明了成熟分化状态的细胞可以被逆转回原始发育状态,同时上述原始发育状态细胞还具有产生一个新个体的能力。这项激动人心的工作让邓宏魁意识到,不久的将来,人类细胞也可能通过细胞重编程进行调控,并有可能开发新的基于细胞的治疗方法。随后,1998年,美国威斯康星大学的研究人员首次建立了人胚胎干细胞系,正式开始了对人类多能干细胞的研究,“再生医学”的大门同时开启。
“这就是我未来想做的事。”这也是当时北大想做的事。一拍即合。
邓宏魁形容最开始在北大做干细胞研究是近乎“白手起家”。没有空间,就临时在一个仓库里面整出个地方,没有网线,就自己去拉,下雨屋子里面还漏水,有时候会停电,停电会把设备搞坏……尽管如此,邓宏魁依然带领团队,在北大完成了世界上第三代干细胞技术,也就是化学小分子技术,为干细胞研究开辟了新的途径。

2013年,邓宏魁团队首次报道仅使用化学小分子将发育成熟的体细胞重编程到多能干细胞,建立了细胞命运调控的化学重编程技术,开辟了全新的细胞命运调控途径
从2013在概念上证明使用小分子处理即可将小鼠体细胞诱导到多能状态,到在化学重编程过程中发现人体细胞中激活的再生基因网络,邓宏魁记得团队每一次发现新的突破点时的振奋。沿着化学小分子技术指出的诸多可能,近些年邓宏魁仍旧在带领团队尝试一些源头上的创新,试图建立一些新的技术方法,为未来再生医学奠定基础。
比如在糖尿病治疗领域,邓宏魁团队所发明的人CiPS细胞可高效增殖、分化为结构和功能与人原代胰岛相似的分化胰岛,有望替代糖尿病患者体内衰竭死亡的胰岛β细胞,成为治疗糖尿病的全新方案。

邓宏魁团队在Nature Medicine上发表《人多能干细胞来源胰岛改善非人灵长类动物的糖尿病》
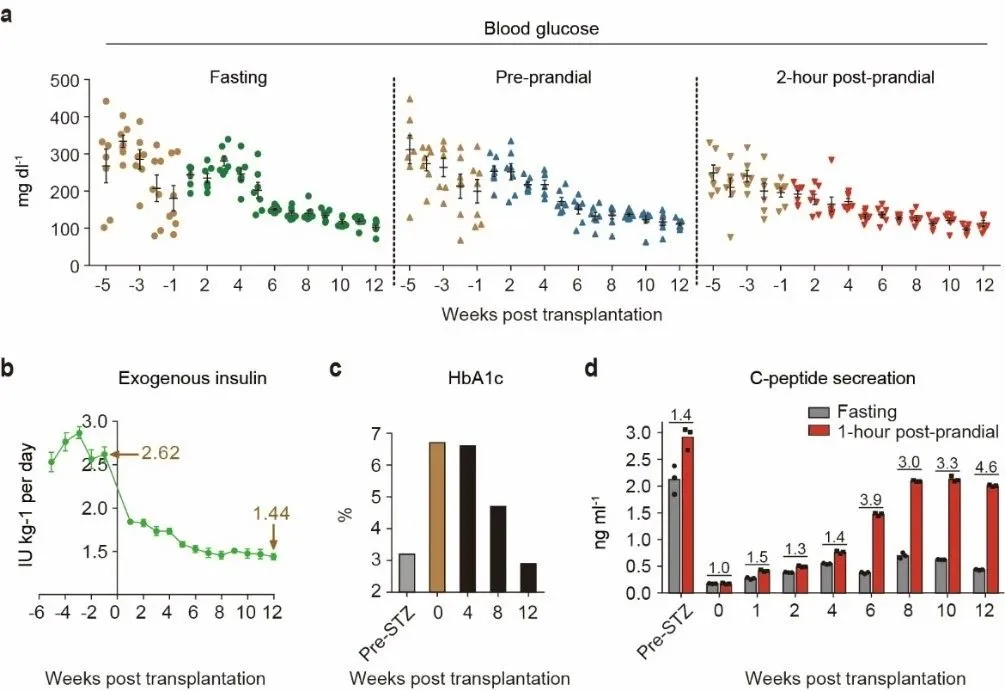
人CiPS细胞分化的胰岛细胞植入腹直肌前鞘后,糖尿病猴血糖控制得到显著改善
而在艾滋病治疗领域,邓宏魁团队也通过在大量动物模型中的尝试,开发出了新的临床治疗手段——通过构建CCR5缺失的人CiPS细胞系,并将这些细胞转化成造血干细胞以供移植使用。虽然该疗法仍然处于开发阶段,但其广阔的应用前景值得期待。
除此之外,在体外肝脏细胞的开发、干细胞与治疗肿瘤免疫学的结合等领域,也能常常看见邓宏魁的名字出现。依托北大提供的交叉平台,邓宏魁在进一步拓展自己的学术所及。
邓宏魁坦言:“我对中国未来研究‘大问题’的进展充满信心,未来生命科学的中心会逐渐转向中国。”
生命要像种子一样,不断生长
与干细胞携手十几年,邓宏魁也尝试用干细胞向大众解释自己:“我是一个特别有激情的人。我觉得人不管到哪个年龄,都要在生长,停止生长就丧失了生命力。这么多年,我的好奇心没有变、激情没有变,这些跟年龄无关,我觉得做科学,这是比较重要的。有点像我研究的干细胞,干细胞里面最重要的一种就叫多能干细胞,能够长出身体内几乎所有的各种组织细胞,就像一个种子,可以不断生长……”
生长,是邓宏魁为自己寻找的基点,源于对生命、对活力本真的热爱。他的目光串联起生命的两端,从起源到衰老。邓宏魁诚恳地说道:“衰老研究是我很感兴趣的一个领域,此外,我对细胞全能性和全能干细胞的体外衍生相关研究也感兴趣。解决上述两个问题能帮助我们理解一个基本生物学问题——生命的起源。”围绕着“生命”这个宏大的话题,邓宏魁进行着细致而具体的工作。
他及团队和合作者共同开发了一种基于增加溶酶体β-半乳糖苷酶活性选择性地清除衰老细胞的前药策略,这为开发抗衰老干预措施提供了新思路;他也报道了一种可在体外维持功能稳定的全能样干细胞的方法,为体外获得全能性干细胞开启了一扇新的大门。
在延伸“生命”研究长度的同时,邓宏魁也在通过综合交叉拓展“生命”研究的宽度。他与化学交叉,与杨震、吴云东等学者合作,多年来一直使用化学生物学的手段研究再生医学;他还与材料学、与工学交叉,一起推进人工肝的装置研究;他也常与临床医学的学者合作,从实验室到医学,用脚步缩减科学研究到临床应用的距离……
从2001年至今,邓宏魁已经在北大扎根24年。24年,他完成了从青年学者到学科领头人的蜕变,而这条成长之路上,依然有无数的后来者。

邓宏魁与课题组成员
邓宏魁真诚地将自己的经验与无数青年学者共享:“我建议青年研究员关注他们研究领域中最重要的问题。如果我能和过去的自己对话,我会告诉自己保持积极、坚持和热情。解决一个棘手的科学问题有助于保持研究的热情和动力,但这个过程本身很具挑战性。对青年研究员来说,坚持和勇气对克服基础研究中可能面临的挑战是最重要的。我也建议他们通过不断地建立广泛的知识体系来为多学科交叉研究和合作做好准备。而且在研究过程中,学术交流非常重要,研究员们需要与其他领域的专家沟通交流,找到潜在的合作机会。同时,这也为他们提供了交流技术、研究方法、科学问题以及从不同角度思考和解决问题的机会。我建议青年研究员们养成学术交流的习惯,这样他们能从其他领域中寻求不同背景专家的意见。”
生命,要像种子一样不断生长。生命科学的研究,也将在一次次如未来科学大奖这样的社会肯定中不断汲取信心。生命科学的中心转向中国,我们拭目以待。

