bat365正版唯一官网
北京大学尹玉新团队揭示DNA损伤修复关键复合物的组装机制
2020年4月24日,北京大学系统生物医学研究所尹玉新团队在Nature Communications发表了题为“Molecular basis for assembly of the shieldin complex and its implications for NHEJ”的研究论文,首次阐释了shieldin复合物的组装机制及其对NHEJ过程的影响。
DNA损伤对基因组稳定性构成了重大威胁,因此细胞利用多种机制来保护其基因组完整性,这些机制统称为DNA损伤反应(DNA damage response,DDR)。在不同类型的损伤中,DNA双链断裂(double-strand breaks,DSBs)是最严重的DNA损伤类型之一。DSB主要通过两种途径进行修复:同源重组(homologous recombination,HR)和非同源末端连接(non-homologous end-joining,NHEJ)。同时,非同源末端连接(NHEJ)还参与抗体类别转换重排(class-switch recombination,CSR),功能障碍端粒融合以及染色体内断裂修复。因此,NHEJ的发生和NHEJ的精细调控对于机体而言至关重要。
同源重组修复(HR)以姐妹染色单体的同源序列为模板进行,依赖于核酸酶对DNA末端切除(resection),产生一长段RPA包裹的单链DNA。非同源末端连接(NHEJ)则不需要模板直接进行末端连接修复,因此必须要抑制DNA末端切除的进行,才能确保NHEJ的顺利进行,而DNA末端切除的抑制机制此前一直是个悬而未决的科学问题。最近多个课题组报道shieldin复合物是位于DNA损伤修复反应53BP1-RIF1通路下游的效应因子,它可以直接结合双链断裂后产生的单链DNA末端,抑制其末端切除,促进NHEJ的转换进行。然而,shieldin复合物的具体组装机制目前尚不清楚。
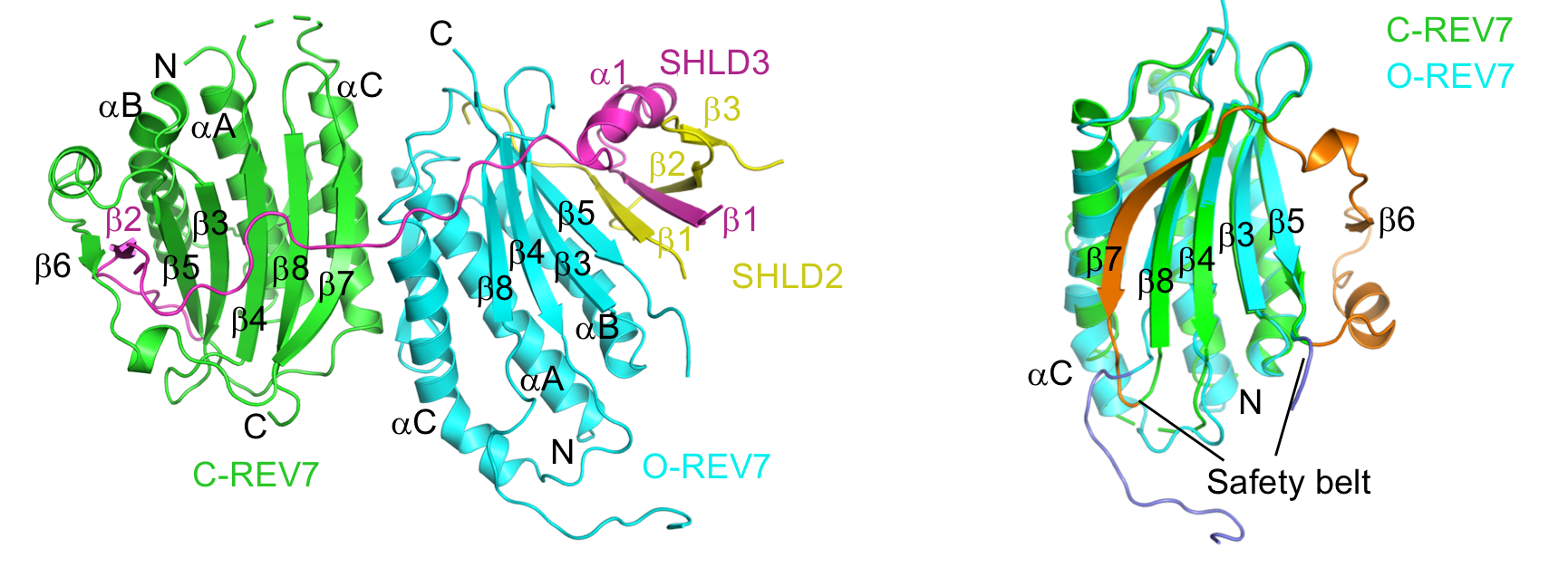
研究团队通过大量的生化鉴定,制备了均一稳定的SHLD3-REV7-SHLD2三元复合物,成功解析了高分辨率的复合物晶体结构。非常重要的是,结构显示此复合物中REV7存在关闭(C-REV7)和开放(O-REV7)两种不同的状态,并且形成C-REV7-O-REV7构象二聚体。进一步实验证实,O-REV7对于shieldin复合物的组装必不可少,构象二聚体界面的关键氨基酸残基的突变可以完全打破两者之间的相互作用并且显著影响NHEJ效率。这是首次发现REV7能够形成构象二聚体,对正确理解REV7分子的工作机制非常关键。
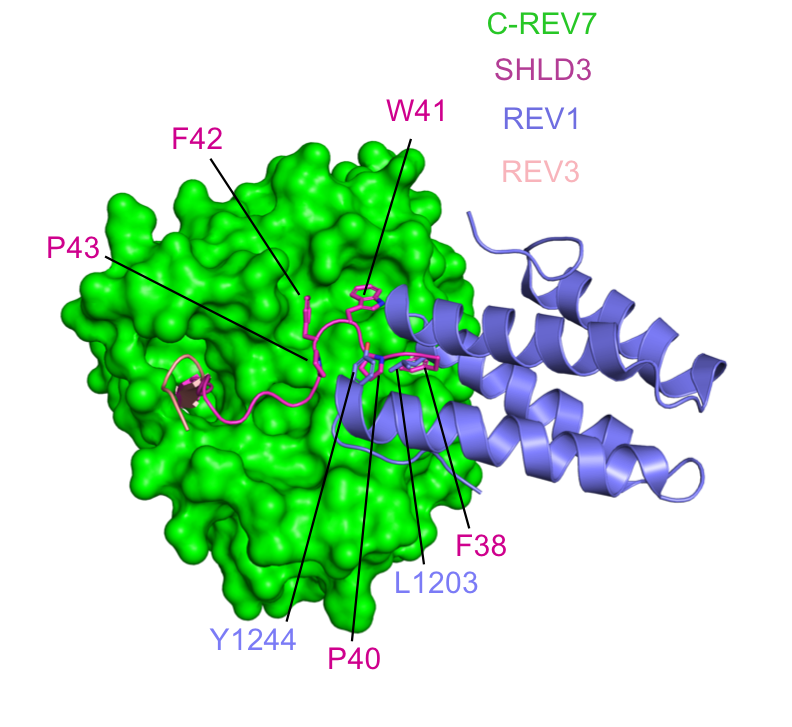
研究人员还发现,SHLD3上非常保守的FXPWFP模体能够结合在C-REV7的表面,这一表面正是跨损伤合成酶REV1结合C-REV7的位置(REV1-REV7复合物的形成易引起肿瘤细胞对化疗药物的不敏感),导致C-REV7只能选择性结合SHLD3或REV1,由此确定了NHEJ和跨损伤合成修复的互斥关系,这为开发增强化疗作用的新型抗肿瘤药物提供了结构基础。
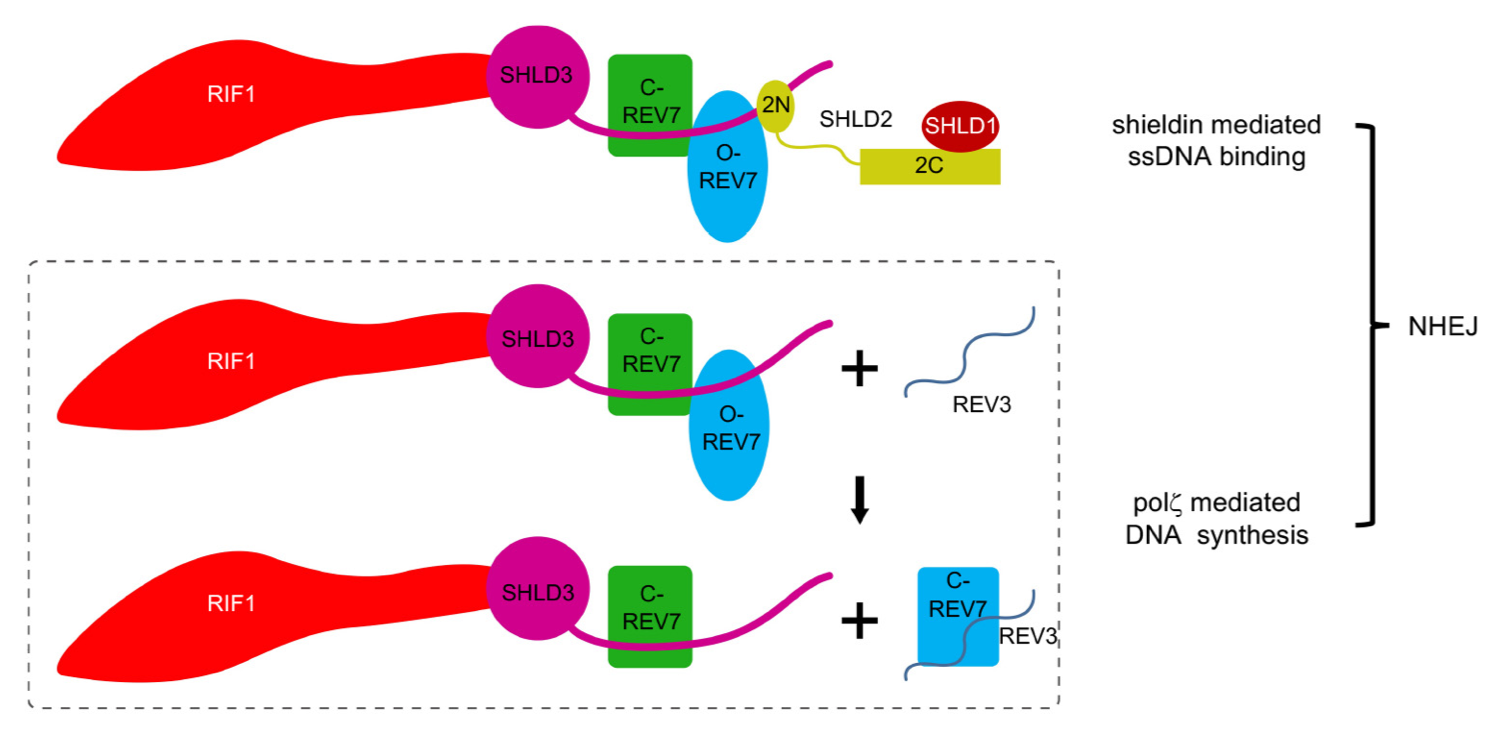
此外,REV7构象二聚体还可能作为平台结合其它DNA修复蛋白分子如REV3。研究人员首次证实在DSBs发生后REV3能够定位到DNA损伤位点,并与REV7构象二聚体发生物理相互作用,促进损伤修复过程。
总之,此项研究阐明了在DNA修复过程中shieldin复合物的组装机制,首次证明了REV7构象二聚体的存在和作用,刷新了学界对REV7分子存在形式的认识,为制定针对DNA损伤修复的肿瘤靶向治疗和化疗策略提供了全新的思路。
北京大学医学部优博培育计划梁令和冯嘉汶博士为该论文的共同第一作者,北京大学系统生物医学研究所尹玉新教授和梁令博士为共同通讯作者。该研究得到了上海张江国家蛋白质科学研究设施晶体衍射线站BL18U1和国家蛋白质科学中心凤凰工程的平台支持。本课题实施过程中,bat365官网登录入口王嘉东研究员和云彩红教授提供了大力支持和帮助,清华大学生命科学学院陈柱成教授以及北京大学物理学院毛有东研究员也给予了指导建议。
尹玉新教授长期从事肿瘤系统生物医学研究,他的研究得到科技部重大专项、国家自然科学基金重点项目、北京市自然科学基金重点项目和北大-清华生命科学联合中心的支持。
相关链接:https://www.nature.com/articles/s41467-020-15879-5
作者简介

尹玉新,北京大学讲席教授,病理学教授,北大-清华生命科学联合中心资深研究员。1997年毕业于美国北卡罗莱纳大学,获分子生物学和遗传学博士学位。1999年加入美国哥伦比亚大学教授系列,2008至2018年任bat365官网登录入口院长,现任北京大学系统生物医学研究所所长,中国病理生理学会系统生物医学专业委员会主任委员。主要研究方向为肿瘤分子生物学与肿瘤免疫学。2008年回国以来,主持了国家基础研究重大项目(973计划)、国家重点研发计划蛋白质机器与生命过程调控重点专项,国家自然科学基金重点项目、北京市自然科学基金重大项目等多项国家及部委级课题,取得了一系列重要成果。目前正深入研究肿瘤微环境和肿瘤发生发展机制,并开发新型肿瘤靶向和肿瘤免疫相关药物。

